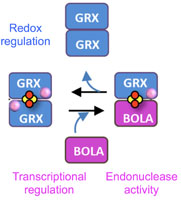
Les glutarédoxines (GRX) ont au moins trois fonctions principales identifiées. Dans les apoformes, elles présentent une activité oxydoréductase contrôlant notamment la glutathionylation / déglutathionylation des protéines. Dans les holoformes, c’est-à-dire les formes de pontage fer-soufre (Fe-S), elles agissent comme des facteurs de maturation pour la biogenèse des protéines à centre Fe-S ou comme régulateurs de l’homéostasie du fer contribuant directement ou indirectement à la détection de l’état du fer cellulaire et/ou sa distribution. Ces dernières fonctions semblent intimement liées à la capacité de GRX spécifiques à former des complexes homodimériques ou hétérodimériques de pontage [2Fe-2S] avec les protéines BOLA. Chez les levures, les deux protéines modulent la localisation et/ou l’activité des facteurs de transcription régulant les gènes codant pour les protéines impliquées dans l’absorption du fer et la séquestration intracellulaire en réponse notamment à une carence en fer. Alors que les isoformes GRX et BOLA des vertébrés peuvent afficher des fonctions similaires, les protéines partenaires impliquées sont différentes. Nous effectuons ici une évaluation critique des résultats soutenant l’implication des deux familles de protéines dans des voies de signalisation similaires dans les plantes et fournissons des idées et des stratégies expérimentales pour délimiter davantage leurs fonctions.
Rey P, Taupin-Broggini M, Couturier J, Vignols F, Rouhier N✉ (2019) Is there a role for glutaredoxins and BOLAs in the perception of the cellular iron status in plants?. Front. Plant Sci., 10:712
